ニュース&イベント NEWS & EVENTS
深層学習で原子間力顕微鏡画像からタンパク質の構造状態が推定可能に
~分子シミュレーション×AIで顕微鏡画像を高精度に解釈~
研究の要旨とポイント
- 高速原子間力顕微鏡画像からタンパク質の構造状態を推定する、新しい深層学習モデル『DeepAFM』を開発しました。
- DeepAFMは、分子シミュレーションで生成した大量の人工データと深層学習を組み合わせることで、ノイズの多い顕微鏡画像から分子の構造状態を推定する手法です。
- DeepAFMを用いて、実験画像の効率的なノイズ除去と分子の状態分類が可能であることを実証しました。
- 本手法はさまざまな生体分子系に応用可能であり、生命科学の発展に貢献することが期待されます。
研究の概要
東京理科大学 理学部第一部 化学科の森 貴治准教授と佐藤 克樹氏(2025年度 修士課程修了)らの研究グループは、名古屋大学大学院 理学研究科 理学専攻の内橋 貴之教授、金岡 優依氏(博士後期課程)、奈良先端科学技術大学院大学の塚崎 智也教授らと共同で、高速原子間力顕微鏡(High-speed atomic force microscopy: HS-AFM、*1)画像からタンパク質の構造状態を推定する新しい画像解析法『DeepAFM』を開発しました。
多くのタンパク質では、機能を発揮する際に開閉運動などの構造変化が伴います。HS-AFMは、このようなタンパク質の動きや状態変化を分子レベルでリアルタイムに観察できる顕微鏡です。しかしながら、HS-AFM画像は一般に解像度が低く、ノイズや歪みを伴うため、タンパク質の詳細な構造状態を正確に読み取ることが難しいという課題がありました。
本研究では、分子の動きを計算機上で再現する「分子動力学シミュレーション(*2)」と、画像解析に広く用いられている「深層学習(*3)」を組み合わせ、HS-AFM画像のノイズや歪みを除去しながらタンパク質の構造状態を推定する新しい手法『DeepAFM』を開発しました。
DeepAFMをタンパク質複合体のHS-AFM画像に適用したところ、画像中のノイズの影響を抑えつつ、タンパク質の重要な運動に関わる領域に主に着目して構造状態を推定していることが示されました。
本研究は、計算科学に基づく「分子シミュレーション」と情報科学に基づく「深層学習」を組み合わせ、実験顕微鏡画像からタンパク質の動きを読み解く新たな画像解析手法を提案するものです。今後、さまざまな生体分子系への応用により、生命科学のさらなる理解につながることが期待されます。
本研究成果は、2026年4月27日に国際学術誌「Journal of Chemical Information and Modeling」66巻8号4484-4498頁に掲載されました。
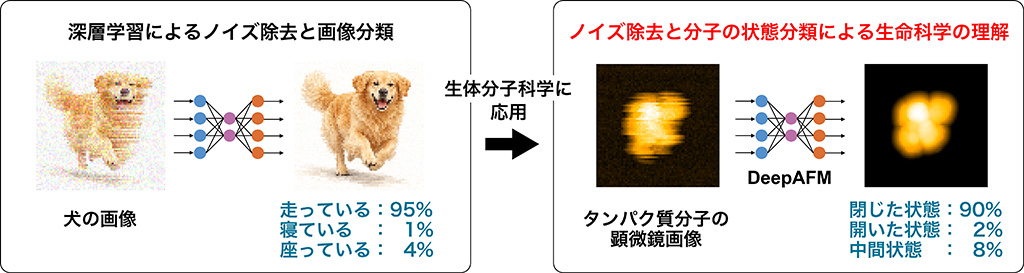
図1. 本研究の概要。深層学習による画像解析技術をタンパク質のHS-AFM画像に応用することで、タンパク質の運動を高精度に解析することが可能になる。
研究の背景
高速原子間力顕微鏡(HS-AFM)は、探針(カンチレバー)で標的タンパク質の表面を高速に走査し、高さの変化を測定することで、単一分子レベルでのタンパク質の動きをミリ秒オーダーでリアルタイムに観察可能にする顕微鏡です。酵素反応や物質輸送などの生命機能に関わるタンパク質の構造変化を、極めて高い時間分解能で直接捉えられることから、生命現象の理解に大きく貢献しています。
一方、HS-AFMは0.1nm程度の極めて高い垂直分解能を誇りますが、水平解像度は依然として限定的(2–3 nm)で、さらに非同時性(タイムラグ)などにより、観察像には歪みが生じる可能性もあります。そのため、画像中のタンパク質の状態を正確に推定するための方法が求められています。従来は、タンパク質の立体構造とシミュレーション画像との類似性に基づき状態を推定する方法(剛体フィッティング法など)が用いられてきましたが、この方法はノイズの影響を受けやすく、推定結果が実際の状態を正しく反映しているか慎重に評価する必要がありました。
近年、画像解析のための手法として「深層学習」がさまざまな分野で活用されており、ノイズ除去や画像分類などの技術が化学や生物学における顕微鏡画像解析にも応用されています。HS-AFM画像に対しても深層学習の応用が始まっていますが、タンパク質の構造は柔軟であるため構造状態の多様性が大きく、さらに実験のみで深層学習に必要な大量の教師データを用意することは一般的に困難です。
そこで本研究では、これらの課題を克服し、画像中のタンパク質の構造状態を推定するための新しい画像解析法を開発しました。
研究結果の詳細
本研究グループはまず、対象とするタンパク質に対して分子動力学シミュレーションを行い、得られる多様な立体構造をもとに大量の人工AFM画像を生成し、画像ごとに状態ラベル(開状態、中間状態、閉状態など)を付与して学習させる教師あり深層学習モデルを構築しました。また、人工AFM画像を生成するアルゴリズムにも、現実的なノイズを模倣するための新たな工夫を導入しました。具体的には、タンパク質の並進運動や回転運動、ピクセル測定の非同時性を考慮することで実験画像に近い特徴を持つ人工AFM画像を生成しました。訓練した深層学習モデルを実験画像に適用することで、画像のノイズ除去とタンパク質の状態分類を同時に実現します。本研究では、この手法を『DeepAFM』と名付けました。
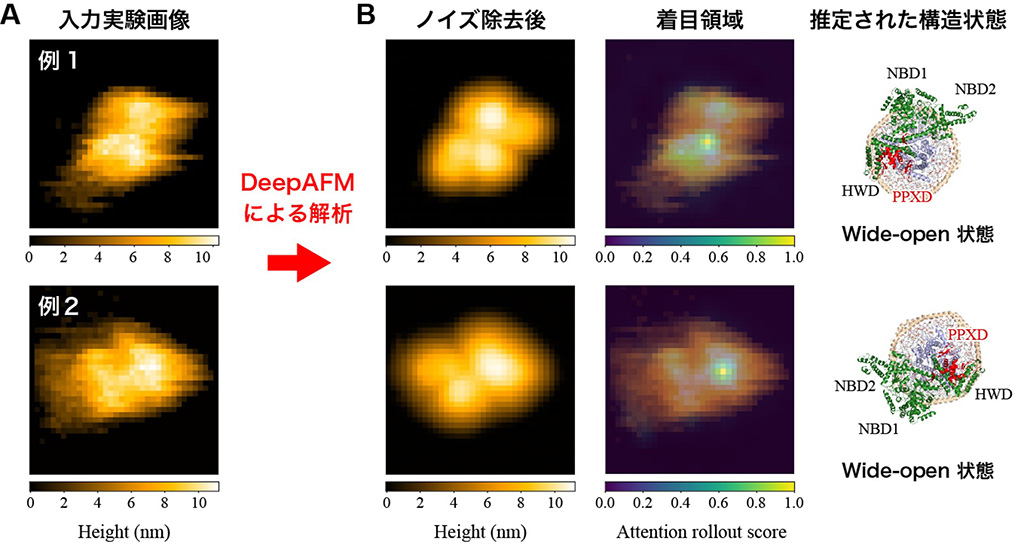
図2. DeepAFMによる入力画像のノイズ除去と膜タンパク質-ナノディスク複合体の構造状態推定。(A) 入力画像、(B) DeepAFMによる解析結果。
着目領域は、深層学習モデルの分類器を構成しているレイヤー内のパラメーターを入力画像に重ね合わせたもの。黄色い領域ほど分類器が注目していることを表している。対象とした膜タンパク質は、タンパク質透過チャネルSecYAEGである。
DeepAFMの性能を評価するために、開閉運動によって物質輸送を行う膜タンパク質のHS-AFM画像を解析しました。実際の実験画像はタンパク質がぼやけたり歪んだりして写っているため、専門家の目で以ってしてもその構造状態を識別することは困難です(図2A)。
DeepAFMをこの実験画像に適用した結果、ノイズを効果的に除去するとともに、タンパク質がドメイン運動をしていると考えられる画像領域に主に着目しながら構造状態を分類し、このタンパク質は大きく開いた構造が主要な状態であると推定しました(図2B)。この推定結果は、他の独立した実験結果とも矛盾しないことが確認され、DeepAFMの妥当性が裏付けられました。
さらに、従来のフィッティング法との比較結果から、本手法はノイズの影響をより受けにくいことも示されました。
本研究は、分子シミュレーションをもとにして生成した大量の人工データと深層学習を組み合わせることで、ノイズの多い顕微鏡画像から分子の構造状態を推定する新しい解析手法です。今後はさまざまな生体分子系への応用や、転移学習を利用したより効率的な解析への発展が期待されます。
本研究を主導した森准教授は、「富岳NEXTを見据え、AIを活用した研究推進を目的として本研究に取り組んできました。本研究を通じて、シミュレーションとAIが人間の解析・解釈を効果的に支援することが期待されます」と、コメントしています。
※ 本研究は、日本学術振興会(JSPS)科学研究費助成事業(JP25K02226, JP24K01309, JP21H05157, JP24K03035, JP25H01329)、革新的ハイパフォーマンス・コンピューティング・インフラ(HPCI) (hp230209, hp240215, hp240277, hp250233, hp250280)、スーパーコンピュータ「富岳」成果創出加速プログラム(JPMXP1020230119)、自然科学研究機構分子科学研究所計算科学研究センター(25-IMS-C151)、科学技術振興機構(JST)Kプログラム(JPMJKP23H2)、ならびに文部科学省(MEXT)「共同利用・共同研究システム形成事業~学際領域展開ハブ形成プログラム~」(JPMXP1323015482)の支援を受けて実施されました。
用語
*1 高速原子間力顕微鏡(High-Speed Atomic Force Microscopy: HS-AFM)
ナノメートルスケールの探針を振動させながら試料表面を高速に走査し、タンパク質など生体分子の形状や動きをリアルタイムで観察できる顕微鏡技術。ミリ秒の時間分解能で単一分子の構造変化を観察できる。
*2 分子動力学シミュレーション(Molecular Dynamics: MD)
原子や分子に働く力を古典力学に基づいて計算し、分子の運動や構造変化をコンピュータ上で再現するシミュレーション法。タンパク質の構造変化や分子間相互作用などの解析に広く用いられる。
*3 深層学習
人工知能(AI)の一種で、多層ニューラルネットワークを用いて大量のデータから特徴を学習する機械学習法。画像認識、音声認識、自然言語処理など多くの分野で利用されている。
論文情報
雑誌名
Journal of Chemical Information and Modeling
論文タイトル
Estimating Protein Conformational States from High-Speed AFM Images with Molecular Dynamics and Deep Learning
著者
Katsuki Sato, Yui Kanaoka, Tomoya Tsukazaki, Takayuki Uchihashi, and Takaharu Mori
