ニュース&イベント NEWS & EVENTS
天然化合物 austocystin D ががん細胞に対して選択的に毒性を発揮するメカニズムを解明
~新規抗がん薬の開発に向けて~
研究の要旨とポイント
- カビ由来の天然化合物 austocystin D が、シトクロム P450 の一種であるCYP2J2を多く発現するがん細胞に、増殖抑制を誘導することは報告されていましたが、その背後にあるメカニズムは不明でした。
- 今回、遺伝子スクリーニングにより、CYP2J2を初めaustocystin Dの細胞毒性に関与する因子とCYP2J2の発現制御因子を同定し、CYP2J2がaustocystin Dの代謝とそれに続く細胞毒性作用に極めて重要であることを明らかにしました。
- CYP2J2 発現レベルの高いがんに対して、 austocystin D やその類縁物質が治療薬として応用できる可能性があります。
研究の概要
東京理科大学大学院 創域理工学研究科 生命生物科学専攻の小島 有紀子氏(2024年度 博士課程3年)、同大学 創域理工学部 生命生物科学科の定家 真人教授らの研究グループは、カビ由来の天然化合物 austocystin D が、シトクロム P450 (CYP)の一種であるCYP2J2を多く発現するがん細胞に、DNA 損傷と増殖抑制を誘導する仕組みを明らかにしました。
これまでの研究から、austocystin D は、CYP依存性のDNA損傷と細胞増殖阻害を誘導することが知られており、austocystin D に高い感受性を示すがん細胞では、CYP2J2の発現上昇がみられます。しかし、austocystin Dの細胞毒性においてどのCYPが関与するか、CYPがどのように関与しているかはまだよくわかっていませんでした。
本研究では、CYP2J2 によって酸化された austocystin D によって DNA 損傷が起こり、細胞死に至るというメカニズムが示されました。austocystin D は正常細胞への毒性は低く、一部のがん細胞に対して選択的な毒性を示すため、新規抗がん薬の開発につながる可能性が期待されています。
本研究成果は、2024年7月15日に国際学術誌「Cancer Science」にオンライン掲載されました。
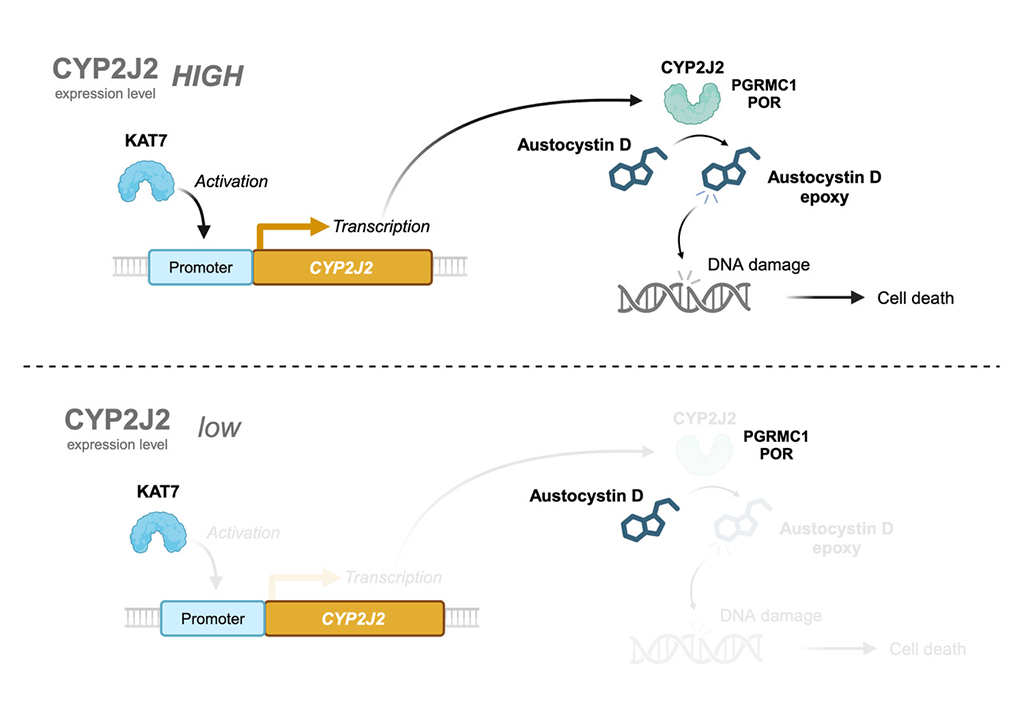
図. austocystin Dによる細胞傷害メカニズムのモデル。
これまでの研究から、austocystin DはCYPにより酸化されたのち、DNA損傷を誘導し、細胞増殖を抑制すると考えられている。本研究ではaustocystin Dによる細胞傷害にCYP2J2が必要であることを示した。KAT7はCYP2J2の転写を促進し、PGRMC1とPORはCYP2J2の酵素活性を補助すると考えられる。CYP2J2発現量の低い細胞においては、austocystin Dは酸化されにくいため、細胞の増殖に悪影響を与えない。
研究の背景
カビ由来の天然化合物である austocystin D は、ヒト細胞に対する細胞毒性を持つ化合物です。austocystin D は正常細胞への毒性は低く、一部のがん細胞に対して選択的な毒性を示すため、新規抗がん薬の開発につながる可能性が期待されています。
これまでの研究から、austocystin D はシトクロム P450(CYP)(*1)によって酸化されることで DNA 損傷を起こし、細胞増殖の抑制を引き起こすと考えられてきました。先行研究では、数百のヒトがん細胞株における化合物の細胞傷害性と遺伝子発現の包括的な相関解析により、austocystin D 感受性とCYP2J2(CYP ファミリーに含まれる酵素)の発現との間に正の相関が見られたと報告されています。このように CYP2J2 が austocystin D の細胞毒性に関わっている可能性が示されてはいるものの、CYP2J2 が寄与するかどうかは未解決のままです。
そこで本研究では、CYP2J2が austocystin D のがん細胞に対する毒性にどのように寄与するか調べました。さらに、遺伝子スクリーニングを通じて austocystin D の細胞毒性に関与する因子および CYP2J2 の発現調節因子を特定し、そのメカニズムを解明しました。
研究結果の詳細
-
CYP2J2 の austocystin D の感受性への寄与
39 種類のヒトがん細胞株の薬物への応答や遺伝子発現プロファイルなどの包括的な情報を含むJapanese Foundation for Cancer Research 39(JFCR39)パネル(*2)のデータを使用しました。その結果、先行研究と同様に、 CYP2J2 の発現は austocystin D の感受性と高い正の相関を示しました。
続いて、austocystin D による DNA 損傷について評価しました。austocystin D処理によって、高レベルに CYP2J2 を発現するU-2 OS 細胞(*3)では DNA 損傷が増加しましたが、発現レベルの低いHOS 細胞(*4)では増加しませんでした。このことは、CYP2J2 を高レベルで発現する細胞では CYP2J2 によって酸化された austocystin D によって DNA 損傷が起こり、細胞死に至ることを示唆しています。
CYP2J2 の過剰発現が austocystin D の細胞毒性を増強するかどうかを調査するために、CYP2J2 をコードする配列を含むレトロウイルスベクターを HOS, SaOS-2(*5), U-2 OS 細胞に導入しました。これらの細胞株は異なるaustocystin D感受性を示しますが、すべての細胞株において、CYP2J2の過剰発現はaustocystin D処理によるDNA損傷誘導や細胞増殖抑制を増強させました。これらの結果は、CYP2J2 が DNA 損傷誘導を伴うaustocystin D の細胞毒性作用に関与していることを示唆しています。
CYP 阻害剤の一種であるケトコナゾールは、がん細胞における austocystin D 感受性を緩和することが知られています。U-2 OS細胞では、austocystin D 処理による生存率の低下やDNA損傷誘導がケトコナゾール処理により緩和されました。また、CYP2J2発現の抑制によって、austocystin D 感受性が緩和されました。
これらの結果から、austocystin D の細胞毒性における CYP2J2 活性の重要性が確認されました。
-
austocystin D 細胞毒性の調節に影響を与える因子の解明
CRISPR-Cas9 gRNA スクリーニング(*6)を実施し、ヒット遺伝子(POR, PGRMC1, KAT7)を得ました。POR は CYP による酸化反応に必要な電子供与体であり、austocystin D は CYP によって酸化されることで DNA 損傷を起こすという仮説を支持します。また、KAT7(転写の調節に寄与する遺伝子)をノックダウンすると、CYP2J2 の発現量が減少することが分かりました。また、マッピングにより、KAT7 は直接的に CYP2J2 の転写を促進し、特定のがん細胞におけるCYP2J2の発現量亢進に寄与している可能性が示されました。
これらの結果から、本研究では austocystin D による細胞毒性には、CYP2J2 が寄与していることが分かりました。本研究により、CYP2J2 発現レベルの高いがんに対し austocystin D やその類縁物質が治療薬として利用できる可能性が示唆されました。
定家教授は、「本研究は、MEXT、AMED主導のがん研究プロジェクトである、次世代がん研究シーズ戦略的育成プログラム(P-DIRECT, 2015年度に終了)に参画していた石川冬木博士(京都大学)のもとで、本プロジェクト推進部、産業技術総合研究所、がん研究会がん研究所などの多大な協力を得て、一部の骨肉腫細胞株の増殖を抑える化合物としてaustocystin Dが見いだされたことに端を発します。年月を経て、研究者を目指す本学学生たちが、学科内教員などの協力を得ながら、本研究を論文という形までまとめ上げたことは大変感慨深いです」とコメントしています。
※本研究は、文部科学省(MEXT)、日本医療研究開発機構(AMED)主導のがん研究プロジェクト『次世代がん研究シーズ戦略的育成プログラム(P-DIRECT)』(JP19H05655)、AMEDの研究費(JP20cm0106113)、JSPS科研費(JP20K07037)、山田科学振興財団、小林財団の助成を受けて実施したものです。
用語
*1 シトクロム P450
ほとんどの生物が持っている酸化還元酵素ファミリーの総称。
*2 Japanese Foundation for Cancer Research 39パネル
公益財団法人がん研究会による、抗がん薬の発見と開発に重要な役割を果たすヒトがん細胞株パネル。
*3 U-2 OS 細胞
ヒト骨肉腫株由来の細胞株。
*4 HOS 細胞
ヒト骨肉腫株由来の細胞株。
*5 SaOS-2 細胞
ヒト骨肉腫株由来の細胞株。
*6 CRISPR-Cas9 gRNA スクリーニング
CRISPR-Cas9による遺伝子ノックアウトを利用した遺伝子スクリーニングのこと。多数の遺伝子をターゲットにした gRNA のライブラリを用意し、目的に応じたスクリーニングを行うことでノックアウトされた遺伝子を特定する。
論文情報
雑誌名
Cancer Science
論文タイトル
Cytochrome P450 2J2 is required for the natural compound austocystin D to elicit cancer cell toxicity
著者
Yukiko Kojima, Saki Fujieda, Liya Zhou, Masahiro Takikawa, Kouji Kuramochi, Toshiki Furuya, Ayaka Mizumoto, Noritaka Kagaya, Teppei Kawahara, Kazuo Shin-ya, Shingo Dan, Akihiro Tomida, Fuyuki Ishikawa, Mahito Sadaie
