ニュース&イベント NEWS & EVENTS
抗うつ薬の効果を高める分子スイッチを発見
日本医科大学
東京理科大学
久留米大学
研究の概要
日本医科大学薬理学の小林克典准教授らの研究グループは、東京理科大学の瀬木(西田)恵里教授、久留米大学の西昭徳教授らの研究グループとの共同研究によって、脳で働く伝達物質ドパミンの受容体を、ノルアドレナリンという別の伝達物質が活性化することによって、抗うつ薬の効果が増強されることを発見しました。
ドパミンの受容体は様々な神経精神疾患やその治療に関与することが知られています。ドパミン受容体はドパミンによって活性化されると一般に考えられていますが、本研究グループはマウスを用いた研究によって、脳の中の海馬と呼ばれる部位では、ドパミンのD1受容体をノルアドレナリンという別の伝達物質が活性化することを発見しました。この作用は運動やストレスなどの影響を受け、運動させたマウスがストレスを受けると、D1受容体がノルアドレナリンによって非常に強く活性化される状態に変化することが分かりました。この変化が起きたマウスに抗うつ薬を投与すると、海馬神経細胞の可塑性注1)が促進され、ストレスによる行動変化が改善することを明らかにしました。つまり、ノルアドレナリン高活性化型のドパミンD1受容体が、抗うつ薬の効果を増強するスイッチとして機能すると考えられます。本研究の成果は、抗うつ薬の治療効果の改善に貢献するとともに、うつ病予防のための生活習慣などの提案に結び付くと考えられます。
本研究成果は、米国科学雑誌「米国科学アカデミー紀要(PNAS)」のオンライン速報版で2022年8月8日の週(米国東部時間)に公開されます。
研究の背景
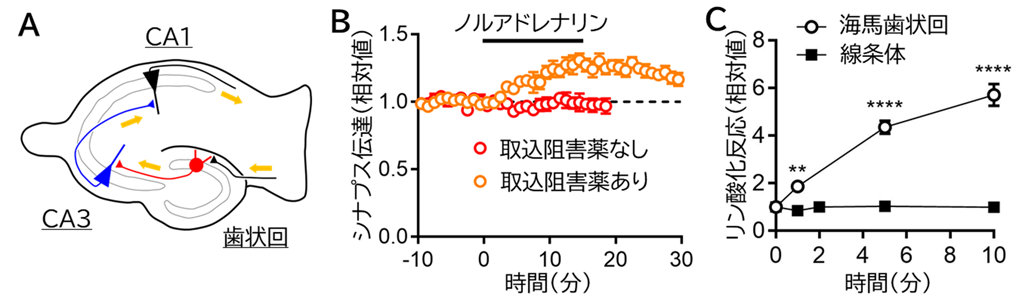
うつ病の治療には抗うつ薬が広く用いられますが、その作用メカニズムの詳細については不明な点が残されています。また、抗うつ薬が有効な治療効果を示さない場合も多く見られ、その理由も明らかではありません。実験動物を用いた研究によって、抗うつ薬の作用には、海馬の歯状回注2)(図1A)が重要な役割を果たすことが報告されています。本研究グループもこれまでに、歯状回の神経細胞が見かけ上若返る「脱成熟」注3)と言う特殊な神経可塑性が、抗うつ作用の基盤であることを提唱しました。この脱成熟を含む、抗うつ薬による歯状回の変化には、ドパミンのD1受容体が寄与することが分かっていました。しかし、海馬にはドパミンを放出する神経線維が少なく、ドパミン量も少ないため、ドパミンによって受容体が充分に活性化されるか明らかではありませんでした。
研究成果の概要
本研究グループは今回、海馬に多く存在するノルアドレナリンという別の伝達物質がD1受容体を活性化する可能性に着目しました。これまでD1受容体の活性化には非常に高濃度のノルアドレナリンを必要とすると考えられていましたが、脳切片標本を用いた電気生理学、生化学解析によって、生理的に妥当な濃度のノルアドレナリンが海馬のD1受容体を活性化することを発見しました(図1B)。この作用は海馬の中でも歯状回の神経細胞で顕著に見られ、運動や神経細胞の活動によってD1受容体が変化することによって、ノルアドレナリンの作用が増強されることも分かりました。一方で、D1受容体が多く存在する線条体注4)ではノルアドレナリンによるD1受容体の活性化は見られなかったため(図1C)、ノルアドレナリン-D1受容体シグナル(以後、NA-D1シグナル)は海馬において特別な役割を持つと考えられます。
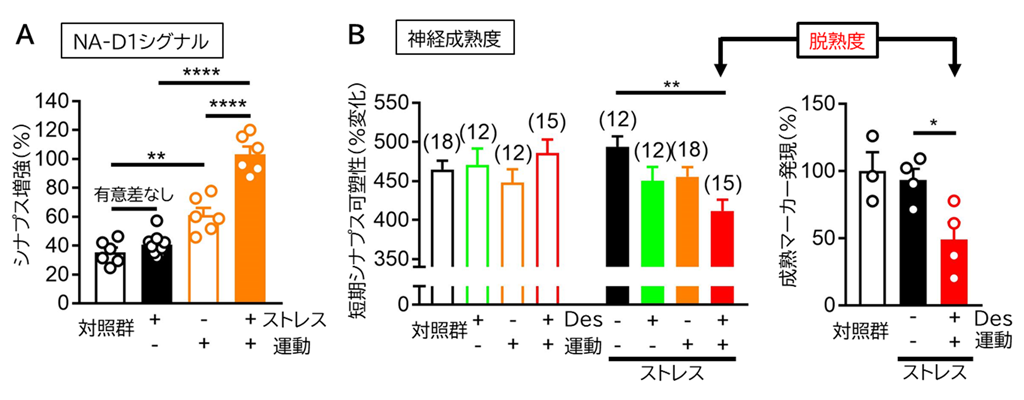
次にストレスをかけたマウスを用いて、抗うつ薬の作用におけるNA-D1シグナルの役割を検討しました。ストレスのみではNA-D1シグナルに大きな変化はありませんでしたが、ストレスをかけたマウスに運動させるとNA-D1シグナルが非常に強く活性化されました(図2A)。このマウスにノルアドレナリン取込阻害作用を持つデシプラミン注5)という抗うつ薬を投与したところ、歯状回神経細胞の脱成熟が誘導されました(図2B)。この脱成熟はD1受容体の遮断によって抑制され、NA-D1シグナルが弱い条件では起きないため、NA-D1シグナルの強度が脱成熟誘導を調節すると考えられます。ストレスをかけるとマウスの自発活動量が低下するうつ病様の行動変化が見られましたが、脱成熟誘導に伴って活動量の低下が回復することも確認されました。以上より、D1受容体がノルアドレナリン高活性化状態に変化することが、抗うつ効果を高めるスイッチとして機能することが示唆されました。
研究の意義・今後の展開
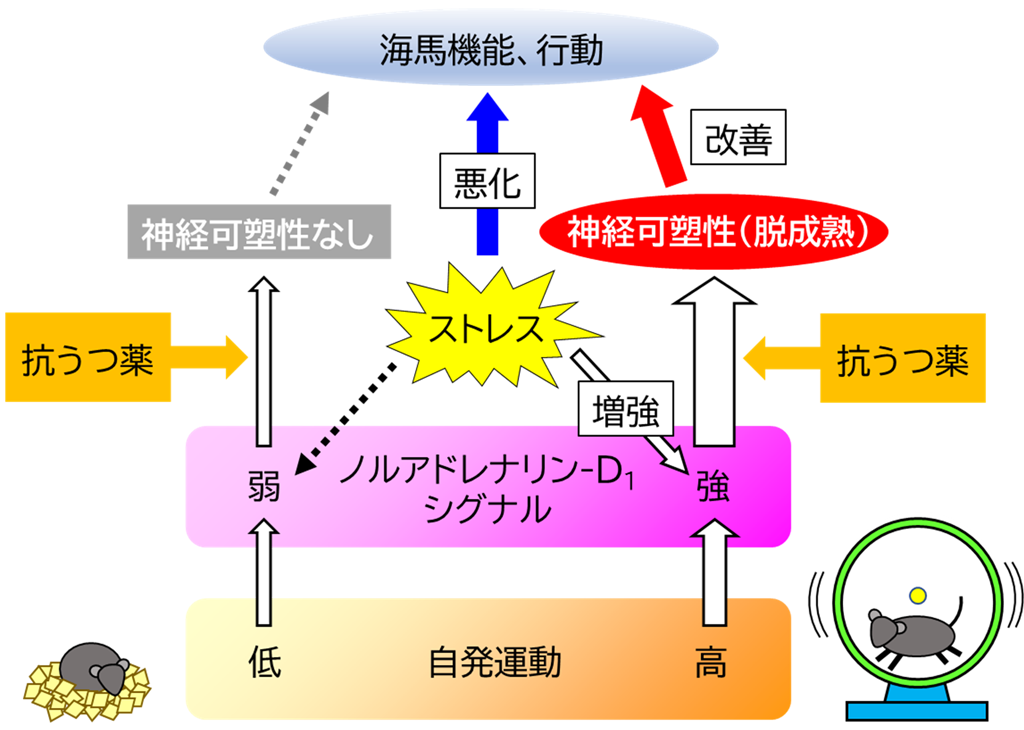
本研究によって、ノルアドレナリンによるドパミンD1受容体の活性化の強さが、抗うつ薬の効果を決定することが示されました(図3)。鍵となるノルアドレナリン高活性化型D1受容体はD1受容体と他の受容体との複合体の可能性が示唆されています。今後分子実体が解明されれば、この受容体を標的としたうつ病治療薬の開発が可能になると考えられます。また、NA-D1シグナルの強化がうつ病予防になる可能性があり、既存の抗うつ薬が効果を示さない場合の増強療法への応用も考えられます。ストレスや運動以外にもNA-D1シグナルに影響する環境、栄養学的要因などがあると予想され、このようなNA-D1シグナルの調節機構の解明が、うつ病治療と予防法の改善につながると期待されます。
用語解説
注1)可塑性
外的な力などが加わって状態が変化した場合に、その変化した状態が持続する性質。
注2)歯状回
認知機能に重要な海馬の一領域で、海馬神経回路の入り口に位置する。近年は精神疾患との関連でも注目されている。
注3)脱成熟
本研究グループが2010年に発見した新しいタイプの神経可塑性。抗うつ薬の慢性投与や、うつ病の電気痙攣療法を模した刺激によって、成熟神経細胞の機能や遺伝子発現が未成熟細胞様に変化する現象。
注4)線条体
ドパミン神経が多く神経線維を送る脳部位であり、運動制御において重要な役割を果たす。
注5)デシプラミン
三環系抗うつ薬の一種。ノルアドレナリン神経終末へのノルアドレナリン取込を阻害することによって、細胞外のノルアドレナリン濃度を上昇させる作用を持つ。
論文情報
雑誌名
Proceedings of the National Academy of Sciences USA
論文タイトル
Noradrenaline activation of hippocampal dopamine D1 receptors promotes antidepressant effects
著者
Katsunori Kobayashi, Kisako Shikano, Mahomi Kuroiwa, Mio Horikawa, Wakana Ito, Akinori Nishi, Eri Segi-Nishida, Hidenori Suzuki
DOI
お問い合わせ
【研究に関するお問い合わせ】
日本医科大学
薬理学教室
准教授 小林 克典
TEL:03-3822-2131(内線:5272)
E-mail:katsu【@】nms.ac.jp
【本プレスリリースに関するお問い合わせ】
日本医科大学 学事部庶務課
TEL:03-3822-2131 FAX:03-3822-8575
E-mail:nms-shomuka【@】nms.ac.jp
東京理科大学 経営企画部広報課
TEL:03-5228-8107 FAX:03-3260-5823
E-mail:koho【@】admin.tus.ac.jp
久留米大学 総合企画部広報室
TEL:0942-31-7511 FAX:0942-31-7718
E-mail:kikakukouhou【@】kurume-ac.jp
【@】は@にご変更ください。
研究室
瀬木研究室のページ:https://eriseginishida.wixsite.com/segi-lab-tokyosci/
瀬木(西田)教授のページ:https://www.tus.ac.jp/academics/teacher/p/index.php?6b43
東京理科大学について
東京理科大学:https://www.tus.ac.jp/
詳しくはこちら
