ニュース&イベント NEWS & EVENTS
食用トウモロコシから、がん細胞増殖抑制効果のあるナノ粒子を作製
~安価で大量に作製できる治療薬として、がん治療などへの応用に期待~
研究の要旨とポイント
- 食用トウモコロシから、簡単な手法で、均一サイズのナノ粒子を大量に作製することに成功しました。この手法は、合成ナノ粒子における生産性とコスト面の問題を解決します。
- 作製したトウモロコシ由来ナノ粒子は、がん細胞に優先的に取り込まれ、がん細胞の増殖を抑えました。また、免疫細胞に作用することにより、がん細胞の増殖をさらに抑制しました。
- ナノ粒子を最適化し、抗がん剤などと組み合わせることにより、安価で安全性の高いがん治療薬または薬物送達担体としての応用が期待されます。
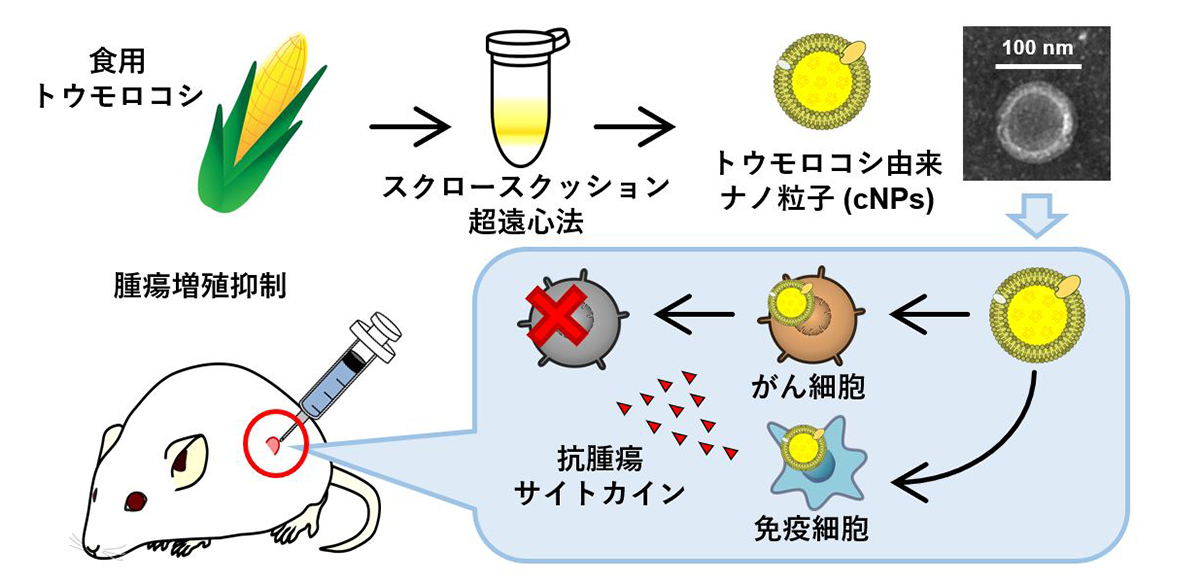
東京理科大学薬学部の西川元也教授、草森浩輔助教、薬学研究科の佐々木大輔氏(博士後期課程1年)らの研究グループは、食用トウモロコシ(スーパースイート種)を用いて、簡単な手法により、均一サイズのナノ粒子を大量に作製することに成功しました。このナノ粒子はがん細胞に優先的に取り込まれ、がん細胞の増殖を抑制しました(図1)。また、免疫細胞に作用することで、さらに強い抗がん効果を発揮しました。このことから、トウモロコシ由来ナノ粒子は、治療薬または薬物送達担体としてがん治療などに応用できると期待されます。
ナノ粒子(Nanoparticles, NPs)とは、リポソームや脂質エマルジョンなど脂質膜で囲まれた直径約100nmのごく小さな粒子のことで、近年盛んに研究が行われ、様々な分野で利用されています。大きさや膜表面の特性を調節することにより体内動態を容易に制御できることから、NPsはがんや炎症部位等目的の部位へ薬物を効率的に送達するドラッグデリバリーシステムとして非常に有用です。しかし、NPsの合成には非常に複雑な工程が必要となり、コストがかかるという問題がありました。
近年、種々の食用植物にもNPsが存在することが明らかになりつつあります。食用植物由来のNPsに共通する特徴として、大きさがナノメートルサイズ、作製方法が簡単、低コストで大量に生産可能なことが挙げられます。また、植物に由来するNPsは様々な生理活性物質を含むことが報告されています。
そこで西川教授らの研究グループは、世界中で広く生産され、様々な遺伝子組換え体も開発されているトウモロコシを材料にNPsを作製し、得られたNPsのもつ生理活性を、細胞およびモデルマウスを用いて確認しました。
本研究成果は、2021年11月24日に国際学術誌「Scientific Reports」にオンライン掲載されました。
研究の背景
NPsの作製方法については様々な研究が行われています。従来から用いられている化学的な合成方法に加えて、近年では細胞外小胞(Extracellular vesicles, EVs)*1と呼ばれる、哺乳類由来の細胞から放出される小さな粒子を用いてNPsを作製する方法が盛んに研究されています。EVsは高い機能性と生体適合性から治療薬として非常に有望ですが、生産性が低いため臨床応用は限られていました。
そこで、西川教授らの研究グループは、生産性の高いNPsの作製方法として食用植物由来NPsに着目しました。研究グループは植物の中でもトウモロコシに注目しました。トウモロコシは私たちの身近なエネルギー源であり、食物繊維やビタミン、必須ミネラルを多く含みます。安価で大量生産が可能であることから、トウモロコシを材料とすることで合成NPsが抱える高いコストと複雑な作製プロセス、そしてEVsが抱える低生産性という問題を全て解決できると期待できます。
研究結果の詳細
トウモロコシ由来NPs(cNPs)を作製するために、まず、トウモロコシ(スーパースイート種)の可食部を粉砕し、粉砕液を遠心分離しました。得られた上清をフィルターでろ過し、60%スクロース溶液を加えて超遠心分離し、スクロース溶液の上層部分に沈降した分画をcNPsとして回収しました(スクロースクッション超遠心法)。
次に、得られたcNPsを動的光散乱分析法(DLS)で分析したところ、平均直径は約80nmで、粒子サイズはほぼ均一でした。また、粒子の表面電荷の指標となるゼータ電位は約-17mVで、これらの値は実験間でほぼ一定であったため、この手法によるcNPsの作製には高い再現性があると言えます。さらに、透過型電子顕微鏡を用いた観察からは、cNPsが脂質二重層の膜からなる中空の構造を有するNPsであることがわかりました。また、トウモロコシ粉砕液1 mLから得られた粒子数は35.6±1.9×1011個であったことから、cNPsは簡単かつ大量に作製できることも確認しました。
得られたcNPsの機能を解明するために、まず、マウス結腸腺がん細胞株colon26(以降、「がん細胞」)、マウス線維芽細胞株NIH3T3(以降、「正常細胞」)、マウスマクロファージ様細胞株RAW264.7(以降、「免疫細胞」)の3種類の細胞を用いて、細胞内への取り込みを調べました。蛍光染色したcNPsを各細胞に添加し、3時間培養した後に観察すると、3種類すべての細胞でcNPsの蛍光が見られましたが、中でもがん細胞に多く取り込まれていました。
一般にNPsはエンドサイトーシス*2によって細胞内に取り込まれることから、4種類のエンドサイトーシス阻害剤(MßCD、CPZ、EIPA、Filipin III)を用いて、がん細胞内への取り込みを調べました。すると、コレステロール依存性エンドサイトーシス阻害剤であるMßCDを加えた場合に最も取り込みが阻害されました。これは、cNPsのがん細胞内への取り込みには、コレステロール依存性エンドサイトーシス経路が大きく関与することを示唆しています。
次に、上記3種類の細胞に0〜1000µg/mLの各濃度のcNPsを添加24時間後の生細胞数は、正常細胞および免疫細胞では大きな変化が見られなかった一方、がん細胞では500µg/mL以上のcNPs添加群では大きく減少しました。ヒト乳がん細胞株MDA-MB-231およびヒト膵がん細胞株Panc-1を用いた実験でも同様の結果が得られました。トウモロコシに含まれるルテインやゼアキサンチンなどのキサントフィル色素は、細胞周期停止やアポトーシス(細胞死)を介して、抗がん作用を有すると報告されており、cNPs中に含まれるこれらの分子がcNPsのこの生物活性に影響を与えている可能性があります。
免疫細胞に対するcNPsの影響を調べると、cNPsを添加した免疫細胞は炎症性サイトカイン*3であるTNF-αを放出しました。TNF-αは、抗がん作用のあるサイトカインとしても知られています。cNPsで処理した免疫細胞をがん細胞と共培養すると、免疫細胞の細胞数に応じてがん細胞が減少しました。トランズウェルアッセイ(多孔質の膜を介した間接的な共培養)を用いて培養すると、免疫細胞、cNPsともに単独でがん細胞数を減少させましたが、組み合わせるとさらに大きく減少させることがわかりました。このことから、cNPsは直接がん細胞を減少させるだけでなく、免疫細胞を活性化することによりがん細胞を減少させると考えられます。
さらに、担がんマウスの皮下腫瘍内に100または300µgのcNPsを連日投与したところ、21日後の腫瘍体積は投与群で対照群よりもはるかに小さく、その差は300µg投与群でより顕著であったことから、cNPsは腫瘍の成長を強く抑制することが示されました。なおcNPsは主な臓器にほとんど毒性を示さず、血清中のALT値、AST値およびクレアチニン値への影響もありませんでした。
西川教授は、「種々の技術を組み合わせることによりcNPsを最適化し、さらに抗がん剤等の薬剤と組み合わせることにより、安価で安全性の高いがん治療薬として応用できると期待されます。食用植物のナノ粒子化によって新たな生理活性が発見されれば、植物を原料とする医薬品開発の歴史に『ナノ粒子化』が加わることになるでしょう」としています。
※本研究は、小野薬品工業株式会社の研究資金支援を受けて実施したものです。
用語
*1 細胞外小胞:細胞から放出される、脂質二重層の膜で囲まれた、核をもたない粒子と定義される。
*2 エンドサイトーシス:細胞外の物質を細胞膜が包み込み、細胞内へと取り込む作用。関与する分子によって、クラスリン依存性、カベオラ依存性、コレステロール依存性エンドサイトーシスなどがある。
*3 サイトカイン:主に免疫系細胞から分泌されるタンパク質で、細胞間の情報伝達を担う分子の総称。生体防御と恒常性維持に重要な機能を果たす。
論文情報
雑誌名
Scientific Reports
論文タイトル
Development of nanoparticles derived from corn as mass producible bionanoparticles with anticancer activity
著者
Daisuke Sasaki, Kosuke Kusamori, Yukiya Takayama, Shoko Itakura, Hiroaki Todo, Makiya Nishikawa
DOI
研究室
西川研究室のページ:https://www.rs.tus.ac.jp/nishikawa_lab/index.html
西川教授のページ:https://www.tus.ac.jp/academics/teacher/p/index.php?6e61
草森助教のページ:https://www.tus.ac.jp/academics/teacher/p/index.php?6EA5
東京理科大学について
東京理科大学:https://www.tus.ac.jp/
詳しくはこちら
