ニュース&イベント NEWS & EVENTS
中枢神経系疾患薬の経鼻投与実現への道を拓く
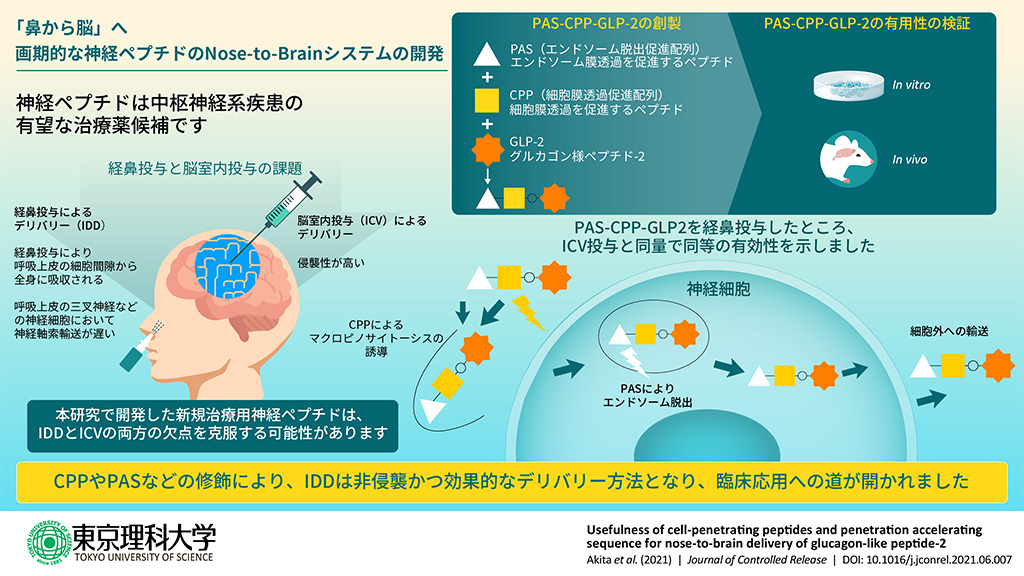
「鼻から脳へ」~画期的な神経ペプチドのNose-to-Brainシステムの開発~
研究の要旨とポイント
- 中枢神経に作用するペプチドは中枢神経系疾患の治療薬として期待されるものの、薬効薬理試験で用いる側脳室内投与は患者への侵襲性が高いことから、非侵襲的な経鼻投与に着目しました。
- 神経ペプチドに機能性配列を付加したペプチド誘導体を新たに創製し、マウスに経鼻投与したところ、側脳室内投与と同じ用量で同等の薬効を発現しました。
- この成果は、うつ病やアルツハイマー病などにも適用可能性があり、汎用性が高く、アンメット・メディカル・ニーズの高い神経変性疾患への適用が期待されます。
東京理科大学薬学部薬学科の山下親正教授、秋田智后助教らの研究グループは、神経ペプチドに機能性配列を付加したペプチド誘導体を新たに創製し、鼻粘膜の呼吸上皮を介した経鼻投与が、ペプチドを中枢神経系(CNS)へ効率的に伝達するドラッグデリバリー経路として非常に有望であることを発見しました。この経鼻投与によるドラッグデリバリーシステム(DDS)は、側脳室内投与と同じ用量でペプチドを効率よくCNSへデリバリーできる新技術です。
薬剤を経鼻投与した場合、体内に取り込まれるルートには、嗅上皮から嗅球を経由して脳に直接到達するルートと、呼吸上皮から体内に取り込まれるルートの2つがよく検討されています。これらに加え、実際には呼吸上皮から三叉神経を介して脳幹(橋)に至る経神経細胞経路もあります。しかし、呼吸上皮は血管系が発達していることから、経鼻投与された薬剤は三叉神経よりもむしろ血中に移行しやすいため、ヒトの鼻粘膜の大部分を占める呼吸上皮から脳に薬剤を届けるためには、呼吸上皮の細胞間隙経路による吸収を抑え、呼吸上皮の三叉神経へ効率良く取り込まれる必要があると山下教授らは考えました。
そこで、本研究では、神経細胞へ効率良く取り込ませるペプチド構造を追求しました。その結果、神経ペプチドに機能性配列(膜透過性促進配列とエンドソーム脱出促進配列)を付加したペプチド誘導体を創製することで、側脳室内投与と同程度に効率良くCNSへ送達させることのできる呼吸上皮の三叉神経を介するCNSデリバリーシステムの構築に成功しました。
このDDS技術は、神経細胞へ薬剤を経鼻的に効率良く取り込ませることが可能であるため、うつ病やアルツハイマー病など、アンメット・メディカル・ニーズの高いCNS疾患への適用が期待されます。
研究の背景
CNS疾患は、アンメットメディカルニーズが非常に高く、近年では治療薬の候補として神経ペプチドを用いた新薬の開発が行われています。しかし、神経ペプチドは、血液脳関門(BBB)を透過することはできません。そこで、薬剤の脳内デリバリーが可能な投与経路としてBBBを回避する経鼻投与が注目されています。
鼻腔内投与後の薬剤の主な伝達経路は、嗅上皮の細胞間隙経路から嗅球を経由して脳に直接送達される経路と、呼吸上皮の細胞間隙経路から全身に吸収される経路の2つがあることが知られています。しかし、げっ歯類では鼻粘膜における嗅上皮が占める割合が約50%であるのに対し、ヒトはその約25分の1の約2%しかないことから、ヒトでは嗅上皮からCNSへの移行経路を介した効率的な中枢移行は期待できません。これらに加え、呼吸上皮から三叉神経を介して脳幹(橋)に至る経細胞経路もありますが、呼吸上皮は血管系が発達していることから、経鼻投与された薬剤は三叉神経よりもむしろ血中に移行しやすく、この特長を活かし全身吸収を企図したペプチド製剤が臨床応用されています。
さらに、神経細胞の軸索輸送が非常に遅いという神経科学の常識があり、殆どのDDS研究者が呼吸上皮の三叉神経からの中枢移行経路にこれまで着目してきませんでした。しかしながら、山下教授らの研究グループでは、ヒトにおいて神経ペプチドを経鼻投与により効率良くCNSへ移行させるためには、DDS研究と神経科学の既成概念を脱却し、呼吸上皮の三叉神経から脳幹(橋)への移行経路に着目することが重要であると考えました。
そこで、本研究では、難治性うつ病に対して抗うつ作用を示す神経ペプチドであるグルカゴン様ペプチド-2(GLP-2)を用いて、神経細胞へ効率良く取り込まれるように、神経細胞への取り込みを促進させる細胞膜透過促進配列(CPP)とエンドソーム膜から脱出を促すエンドソーム脱出促進配列(PAS)を付加したGLP-2誘導体を創製し、この誘導体を経鼻投与すると、側脳室内投与と同じ用量で、しかも既存薬の課題を解決した即効性のある抗うつ様作用を発現することを見出しました。
研究結果の詳細
山下教授らの研究グループは、新しい概念に基づいたCPPとPASをGLP-2に付加したPAS-CPP-GLP-2誘導体を創製しました。この誘導体を用いて、新しい概念に基づいたNose-to-Brainシステムを検証するために、in vitro及びin vivoの両面から検討を行いました。
本研究では、まず、何も修飾していないGLP-2とPAS-CPP-GLP-2をタンパク質分解酵素DPP-IVと一緒にインキュベートして経時変化を調べました。その結果、6時間後にはGLP-2は大半が分解された一方で、PAS-CPP-GLP-2は97.6%が変化せず、非常に安定性が高いことを確認しました。
in vitroの実験からは、エンドサイトーシスの一種であるマクロピノサイトーシスにより、PAS-CPP-GLP-2およびCPP-GLP-2が、神経細胞内へ取り込まれることを明らかにしました。細胞内小器官特異的な蛍光マーカーで染色することで、CPP-GLP-2とPAS-CPP-GLP-2の両方が初期エンドソームに共局在することがわかりました。染色像からエンドソーム脱出効率を算出した結果、PAS-CPP-GLP-2はCPP-GLP-2よりも有意に高いエンドソーム脱出効率を示しました。このことから、神経細胞に取り込まれたPAS-CPP-GLP-2が、効率的に細胞質へ移行することが明らかになりました。一方、CPP-GLP-2はPAS-CPP-GLP-2よりも分解系であるエンドリソソームにより多く局在していることも明らかになりました。
次に、マイクロチャンバーでの神経細胞の培養系を用いて、PAS-CPP-GLP-2の細胞内から細胞外への移行を1細胞レベルで検証しました。これにより、細胞内に取り込まれたPAS-CPP-GLP-2が、細胞外へ排出されることが明らかになりました。
次に、PAS-CPP-GLP-2などの誘導体の薬効をin vivoで検証しました。PAS-CPP-GLP-2をマウスに経鼻投与した20分後に、行動実験により抗うつ様効果を評価したところ、有意な効果があることが示されました。さらに、薬効用量を側脳室内投与および経鼻投与で比較したところ、同じ用量で同等の薬効を示すことが明らかになりました。また、尾静脈内投与により有効性を同様に評価した結果、薬理効果を示さないことが示され、経鼻投与が全身循環に移行した可能性は否定されました。
以上の結果から、ペプチド誘導体PAS-CPP-GLP-2は、PASおよびCPPを付加されたことで、経鼻投与により直接CNSに送達され、これまでの侵襲的な側脳室投与と同等の薬効を発現すること確認しました。
経鼻投与により、効率良くペプチドをCNSへデリバリーできる新規Nose-to-Brain技術を開発することに成功した本成果は、DDS研究と神経科学の既成概念を覆す新しい概念のCNSデリバリー技術開発に資するものです。
山下教授は「現在、このDDSを用いて、うつ病だけでなく、アルツハイマー病などへの適用できる可能性を示唆するデータも得られつつあります。汎用性の高さに加え、神経細胞へ効率良く取り込まれるため、アンメット・メディカル・ニーズの高いCNS疾患への適用が期待されます」と今後の応用の可能性を示しています。
※本研究は、第一三共株式会社共同研究公募プログラムTaNeDS(タネデス)および先進医薬研究振興財団の助成を受けて実施したものです。
論文情報
雑誌名
Journal of Controlled Release
論文タイトル
Usefulness of cell-penetrating peptides and penetration accelerating sequence for nose-to-brain delivery of glucagon-like peptide-2
著者
Tomomi Akita, Ryosuke Kimura, Saki Akaguma, Mio Nagai, Yusuke Nakao, Mamiko Tsugane, Hiroaki Suzuki, Jun-ichiro Oka, Chikamasa Yamashita
DOI
研究室
山下教授のページ:https://www.tus.ac.jp/academics/teacher/p/index.php?64DC
秋田助教のページ:https://www.tus.ac.jp/academics/teacher/p/index.php?6ED0
東京理科大学について
東京理科大学:https://www.tus.ac.jp/
詳しくはこちら
