ニュース&イベント NEWS & EVENTS
短鎖脂肪酸がアレルギーを抑制する作用機構を解明
~アレルギーに対する食物繊維の有効性を分子レベルで実証~
研究の要旨とポイント
- 腸内細菌によって食物繊維から生成される短鎖脂肪酸は、免疫調節機能を有し、アレルギー反応を抑制することが知られていますが、その作用機構については未解明のままでした。
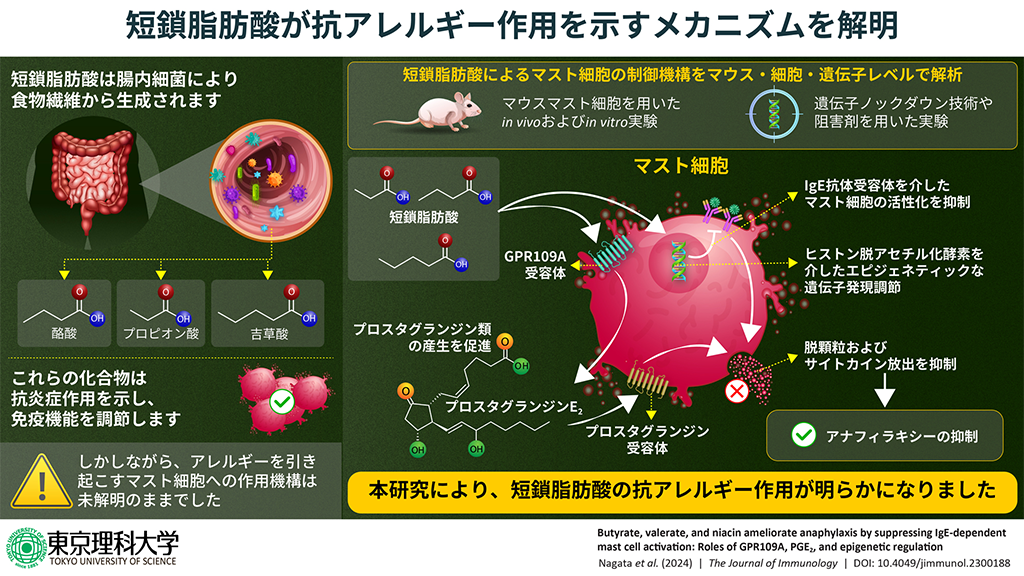
- 短鎖脂肪酸がマスト細胞を介してアレルギー抑制作用を発揮する際の分子機構を、マウス・細胞・遺伝子レベルの解析を組み合わせることで解明しました。
- マウスを用いた実験から、短鎖脂肪酸およびナイアシンがアナフィラキシーを改善すること、NSAIDsがその改善効果を阻害することを明らかにしました。
- 本研究は、私たちが日常的に口にする食事の内容が健康に影響を及ぼすことを、科学的根拠をもって示した重要な成果で、食事内容の見直しや提案にもつながると期待されます。
研究の概要
東京理科大学先進工学部生命システム工学科の西山千春教授らの研究グループは、短鎖脂肪酸が示すアレルギー抑制作用について、マウス・細胞・遺伝子レベルの解析を組み合わせることにより、その詳細な作用機構の解明に成功しました。本研究により、短鎖脂肪酸および食物繊維が持つ抗アレルギー作用の背景にあるメカニズムが明らかになりました。
短鎖脂肪酸(*1)は、主に食物繊維が腸内細菌によって代謝される際に生成される物質で、酪酸や吉草酸、プロピオン酸、酢酸などの総称です。近年の研究から、短鎖脂肪酸には、免疫細胞であるマスト細胞(*2)のはたらきを調節し、アレルギー反応を抑制する機能があることが明らかになりました。しかしながら、短鎖脂肪酸がマスト細胞に作用するその分子機構については未解明のままでした。
西山教授らの研究の結果、短鎖脂肪酸を経口摂取したマウスでは、アナフィラキシー(強いアレルギー反応)が有意に改善されること、また、短鎖脂肪酸とともに培養したマスト細胞では、IgE抗体(*3)により誘導される活性化が有意に抑制されることが明らかになりました。さらに、各種阻害剤や遺伝子技術を用いた解析から、短鎖脂肪酸によるマスト細胞活性化抑制に関与する2つの経路、すなわち「Gタンパク質共役型受容体(*4)GPR109Aを介する経路」と、「免疫関連遺伝子のエピジェネティック(*5)な発現調節を介する経路」が見出されました。
今回、短鎖脂肪酸の受容体として同定されたGPR109Aは、ビタミンB群の一種であるナイアシン(*6)の受容体として知られ、免疫や炎症誘導にはたらくプロスタグランジン(*7)の合成に関与します。本研究では、短鎖脂肪酸同様、ナイアシンがマウスにおけるアナフィラキシーを改善し、プロスタグランジンの合成を阻害する非ステロイド性抗炎症薬(NSAIDs)(*8)が、その改善効果を阻害することも明らかになりました。
本研究成果は、2024年1月10日に国際学術誌「The Journal of Immunology」にオンライン掲載されました。
研究の背景
マスト細胞は、主にアレルギー反応やアナフィラキシーに関与する免疫細胞です。マスト細胞の表面には、IgE抗体の受容体(FcεRI)が発現しています。このFcεRIにIgE抗体が結合し、さらに抗原が結合すること、すなわちIgE抗体と抗原を介して複数のFcεRIが連結(架橋)することで、マスト細胞が活性化されます。マスト細胞は、細胞内に多くの分泌顆粒(*9)をもち、活性化すると、分泌顆粒が細胞外に放出される脱顆粒と呼ばれる現象が生じ、ヒスタミンなどのアレルギー誘因物質を細胞外に大量に放出します。これにより、アレルギー反応が引き起こされます。
西山教授の研究グループでは、食品中に含まれる成分やその腸内代謝産物などが免疫応答に与える影響について研究しています。今回、西山教授らは、抗アレルギー作用を示すことが知られている短鎖脂肪酸に着目して研究を行いました。近年、短鎖脂肪酸がマスト細胞の機能を調節することで抗アレルギー作用を示すというデータが蓄積しつつありますが、その背景にある分子的なメカニズムの詳細はまだわかっていませんでした。そこで本研究グループは、マウス・細胞・遺伝子レベルの解析を駆使して、短鎖脂肪酸がアレルギー反応のエフェクター細胞であるマスト細胞の機能をどのように調整しているのかについて調べました。
研究結果の詳細
まず、受動的全身性アナフィラキシーモデル(IgE抗体を投与し、その後に抗原を投与することで、マウスにアナフィラキシーを誘導するもの)を用いて、マウス生体に対する短鎖脂肪酸の効果を評価しました。すると、短鎖脂肪酸(酪酸、吉草酸)を4~6日間経口投与したマウスでは、アナフィラキシーが有意に抑制されることがわかりました。また、受動的皮膚アナフィラキシーモデル(同様の手法で足底の皮膚にアナフィラキシーを誘導するもの)を用いた場合にも、短鎖脂肪酸の経口投与により、アナフィラキシーが抑制されました。
次に、骨髄由来のマスト細胞を短鎖脂肪酸とともに培養し、マスト細胞に対する短鎖脂肪酸の効果を評価しました。すると、短鎖脂肪酸(特に酪酸、吉草酸、プロピオン酸、イソ吉草酸)で前処理したマスト細胞では、IgE抗体により誘導される脱顆粒が抑制されることがわかりました。また、各種サイトカイン(*10)の放出も、有意に減少することがわかりました。さらに、フローサイトメトリー法および定量的PCR法を用いた実験から、短鎖脂肪酸は、FcεRI関連遺伝子の転写を阻害することなく、細胞表面のFcεRI発現量を減少させることが示されました。
さらに、短鎖脂肪酸の作用機構を解明するべく、定量的PCR法を用いて、マスト細胞上の膜輸送タンパク質や受容体を調べました。同定されたものの中から、各種阻害剤や遺伝子技術を用いた実験により、短鎖脂肪酸の受容体としてGタンパク質共役型受容体GPR109Aが絞り込まれました。
短鎖脂肪酸が示す抗炎症作用には、ヒストン脱アセチル化酵素阻害剤(HDACi)(*11)としての活性が関与することが報告されています。そこで、HDACiの一種トリコスタチンAでマスト細胞を処理し、脱顆粒の程度、サイトカイン放出量、FcεRIのmRNA量、およびマスト細胞表面に発現したFcεRI量を調べたところ、短鎖脂肪酸で処理した場合と同様の結果が得られました。以上の結果から、短鎖脂肪酸の作用機構には、細胞表面に発現するGタンパク質共役型受容体GPR109Aを介する経路と、HDACiとして免疫関連遺伝子の発現をエピジェネティックに調節する経路、これら2つの経路が関与することが示されました。
今回短鎖脂肪酸の受容体として同定されたGPR109Aは、ニコチン酸(ナイアシン・ビタミンB3の一種)の受容体として知られ、ニコチン酸と結合することでプロスタグランジンの産生を促進します。そこで、プロスタグランジンの合成を阻害するNSAIDs(アセチルサリチル酸、インドメタシン)でマスト細胞を処理したところ、短鎖脂肪酸による脱顆粒抑制効果が阻害されました。また、受動的皮膚アナフィラキシーモデルにおいて、ニコチン酸の効果を評価したところ、ニコチン酸はアナフィラキシーを有意に抑制し、その効果はNSAIDsによって打ち消されました。さらに、受動的全身性アナフィラキシーモデルにおける、短鎖脂肪酸のアナフィラキシー抑制効果も、NSAIDsによって阻害されました。加えて、NSAIDsの作用に関する詳細な解析により、プロスタグランジンのうち、特にプロスタグランジンE2がマスト細胞の活性化を抑えること、複数あるプロスタグランジンE2受容体のうちEP3がアナフィラキシーの抑制に関わること、短鎖脂肪酸やニコチン酸の効果がEP3阻害剤によって減弱化することなども示唆されています。これら一連の結果から、短鎖脂肪酸は、受容体GPR109Aを介してプロスタグランジンの産生を促進することで、マスト細胞の活性化を抑制し、アナフィラキシーの抑制にはたらくことが示されました。
本研究成果について、西山教授は「本研究は、日本人の2人に1人が何らかのアレルギーを持つと言われるほど身近な疾患であるアレルギーに対する、食物繊維の有効性を明らかにするものです。NSAIDsは、喘息や炎症性腸疾患などの一部のアレルギーや炎症疾患において憎悪化をもたらすことが知られており、今回の知見は、その点にも切り込んだものです。さらに、アレルギーに対するビタミンの影響も確認されましたが、プロスタグランジンの合成には多価不飽和脂肪酸が関係することや分岐鎖脂肪酸は納豆などにも含まれていることを踏まえても、食事や日常生活と関連の深いテーマとなったと思います」と語っています。
※本研究は、日本学術振興会科学研究費補助金基盤研究(B)(23H02167、20H02939)、基盤研究(C)(21K05297、19K05884、19K08920)、特別研究員(DC2)、特別研究員奨励費(21J12113)、日本免疫学会「きぼう」プロジェクト、東京理科大学学長研究推進助成、飯島藤十郎記念食品科学振興財団、三島海雲記念財団学術研究奨励金、および武田科学振興財団生命科学研究助成の助成を受けて実施したものです。
用語
- *1
-
短鎖脂肪酸
主に腸内細菌によって水溶性食物繊維やオリゴ糖が代謝されることで生成する有機酸の総称。腸管から吸収されて腸上皮細胞のエネルギー源として利用されるほか、血流に乗って全身に運ばれ、肝臓や筋肉での代謝に利用される。短鎖脂肪酸には、腸内を弱酸性に保ち、有害な菌の増殖を阻害することで、腸内環境を良好に保つ機能もある。 - *2
-
マスト細胞
皮膚や粘膜など主に外界と接した組織に多く分布し、本来は寄生虫や細菌などの感染防御に機能する免疫細胞。肥満細胞とも呼ばれる。 - *3
-
IgE抗体
免疫グロブリンEから構成される抗体。特定のアレルゲン(抗原)が体内に侵入した際に産生され、即時的なアレルギー反応を引き起こす。 - *4
-
Gタンパク質共役型受容体
神経伝達物質やホルモンなどを認識する、細胞膜上の受容体。Gタンパク質の活性化を介して、細胞外の情報を細胞内に伝えるはたらきをもつ。 - *5
-
エピジェネティック
DNAの塩基配列を変えることなく、DNAやヒストンの化学修飾(メチル化、アセチル化など)を介して遺伝子の発現を制御する。 - *6
-
ナイアシン
ビタミンB群の一種(ビタミンB3)であり、ニコチン酸とニコチンアミドの総称。 - *7
-
プロスタグランジン
基質となるアラキドン酸から、酵素であるシクロオキシゲナーゼ(COX)によって生成される生理活性物質。PGE2、PGD2などの種類があり、それぞれに異なる機能をもつ。 - *8
-
非ステロイド性抗炎症薬(NSAIDs, Non-steroidal anti-inflammatory drugs)
アラキドン酸カスケードにおいてCOXを阻害し、プロスタグランジンの合成を抑制することで、鎮痛・解熱・抗炎症作用を示す。アセチルサリチル酸(アスピリン)やインドメタシンなどがある。 - *9
-
分泌顆粒
分泌細胞内にみられる小さな顆粒。顆粒内部には分泌物が蓄えられている。 - *10
-
サイトカイン
細胞間の情報伝達にはたらくタンパク質。インターロイキン(IL)や腫瘍壊死因子(TNF)などがある。 - *11
-
ヒストン脱アセチル化酵素阻害剤(HDACi, Histone deacetylase inhibitor)
一般にヒストンがアセチル化されると、転写因子が染色体に近づきやすくなり、転写が促進される。HDACiはヒストンの脱アセチル化を阻害するため、ヒストンのアセチル化、ひいては転写を促進する。
論文情報
雑誌名
The Journal of Immunology
論文タイトル
Butyrate, valerate, and niacin ameliorate anaphylaxis by suppressing IgE-dependent mast cell activation: Roles of GPR109A, PGE2, and epigenetic regulation
著者
Kazuki Nagata, Daisuke Ando, Tsubasa Ashikari, Kandai Ito, Ryosuke Miura, Izumi Fujigaki, Yuki Goto, Miki Ando, Naoto Ito, Hibiki Kawazoe, Yuki Iizuka, Mariko Inoue, Takuya Yashiro, Masakazu Hachisu, Kazumi Kasakura, Chiharu Nishiyama
DOI
発表者
- 長田 和樹*
- 東京理科大学 先進工学部 西山研究室 助教
- 安藤 大介*
- 東京理科大学 先進工学部 西山研究室 修士課程修了(2022年度修士修了)
- 芦刈 翼
- 東京理科大学 先進工学部 西山研究室 修士課程修了(2022年度修士修了)
- 伊藤 莞大
- 東京理科大学 先進工学部 西山研究室 修士課程1年
- 三浦 亮介
- 東京理科大学 先進工学部 西山研究室 博士研究員(当時)
- 藤垣 泉
- 東京理科大学 先進工学部 西山研究室 修士課程修了(2017年度修士修了)
- 後藤 有貴
- 東京理科大学 先進工学部 西山研究室 修士課程2年
- 安藤 実希
- 東京理科大学 先進工学部 西山研究室 修士課程修了(2022年度修士修了)
- 伊藤 直人
- 東京理科大学 先進工学部 西山研究室 博士課程2年
- 川添 響
- 東京理科大学 先進工学部 西山研究室 修士課程修了(2022年度修士修了)
- 飯塚 雄輝
- 東京理科大学 先進工学部 西山研究室 修士課程修了(2019年度修士修了)
- 井上 真理子
- 東京理科大学 先進工学部 西山研究室 修士課程修了(2020年度修士修了)
- 八代 拓也
- 東京理科大学 先進工学部 西山研究室 講師(当時)
- 八須 匡和
- 東京理科大学 先進工学部 西山研究室 講師(当時)
- 笠倉 和巳
- 東京理科大学 先進工学部 西山研究室 博士研究員(当時)
- 西山 千春
- 東京理科大学 先進工学部 教授
*筆頭著者(長田、安藤は同等)
