ニュース&イベント NEWS & EVENTS
オートファジーががん細胞を排除することを発見、新たながん治療法開発に期待
~細胞競合によるがん細胞除去におけるオートファジーの役割を解明~
研究の要旨
- 近年、腫瘍発生を防ぐ仕組みとして、上皮層に発生したがん変異細胞を正常上皮細胞が排除する細胞競合という生命現象が注目されています。しかし、細胞競合を制御する分⼦論的メカニズムの全容は解明されていません。
- 今回、正常細胞に囲まれたがん変異細胞内ではリソソームの機能が低下し、オートファゴソームが蓄積することが細胞競合によるがん変異細胞の排除に必要であることを明らかにしました。
- がんが進⾏した中・後期では、オートファジーはがん細胞の⽣存・増殖を助⻑しますが、超初期では細胞競合を介して抗腫瘍的に機能することが本研究より明らかになったことから、今後、がんの進⾏時期を考慮した制がん戦略が必要になると考えられます。
東京理科大学生命医科学研究所の昆俊亮講師、明果瑠いるま氏(博士課程1年)らの研究グループは、細胞競合によりがん変異細胞が排除されるために、がん変異細胞内のリソソームの機能が障害されることによって、オートファゴソームが蓄積することが必要であることを明らかにしました。
がんが進⾏した中・後期では、オートファジーはがん細胞の⽣存・増殖を助⻑するのに対し、進行初期では抗腫瘍的に機能することがこれまでに示唆されてきましたが、その機序についてはよく分かっていませんでした。そこで研究グループは、がんの超初期でがん変異細胞排除に重要な役割を果たす細胞競合(*1)に着目し、細胞競合におけるオートファジーの役割について詳細に解析を行いました。
その結果、正常細胞に囲まれたがん変異細胞ではリソソーム(*2)の機能が低下し、オートファゴソーム(*3)が蓄積することを⾒出しました。さらに、リソソームの機能を⼈為的に回復させたとき、さらにはオートファゴソームの形成を阻害させるとがん変異細胞は細胞競合により排除されないことから、オートファゴソームの⾮分解機能が細胞競合に必要であることが分かりました。マウス膵管を用いた実験では、オートファゴソームの形成が阻害されたがん変異細胞は膵管より排除されにくくなり、膵管構造が破綻することにより慢性膵炎様病変が引き起こされることが示されました。これらの結果から、オートファジーは細胞競合を介してがん変異細胞を排除することにより、⽣体内の恒常性維持に寄与することが示唆されました。
この研究結果は、がん変異細胞が誕⽣した超初期において、オートファジーは細胞競合を介してがん変異細胞を排除することを⾒出した成果であり、新たながん治療法の開発に繋がることが期待されます。
本研究成果は、2022年8月30日(現地時間)に国際学術誌「Cell Reports」にオンライン掲載されました。
研究の背景
がんは正常細胞の遺伝子変異を端緒に発生します。がん細胞の発生自体は特別なことではなく、体中の至る所で日常的にがん変異細胞が産生されていることが、最近のゲノミクス研究から示されています。それでも多くの場合がん発病に至らないのは、発生したがん細胞を排除する機構が生体内に備わっているためです。そうした機構の一つが、正常上皮細胞ががん変異細胞を排除する現象である細胞競合です。
研究グループはこれまでに、正常上皮層にがん原遺伝子であるRas(*4)の活性化変異体を導入した変異細胞を少数産生させると、正常上皮細胞とRas変異細胞との細胞競合の結果、変異細胞が敗者細胞として管腔側に排除されることを培養細胞もしくはマウス腸管を用いた実験から示してきました(Kon et al., Nat. Cell Biol., 2017)。このように、細胞競合とは偶発的に産生されたがん変異細胞を隣接する正常上皮細胞が認識し、排除するというこれまでに知られていなかった抗腫瘍機能であるため、広範な分野から注目を集めています。しかしながら、細胞競合を制御する分子論的メカニズムの全容は解明されていません。
一方、オートファジーは、細胞内の異常なタンパク質や小器官を分解・リサイクルする品質管理機構で、様々な疾患の発症に関与します。がんが進行した中・後期では、がん細胞の生存・増殖をオートファジーは助長するのに対し、がんの初期では抗腫瘍的に機能することがこれまでに示唆されてきましたが、その機序についてはまだよく分かっていませんでした。そこで本研究では、細胞競合におけるオートファジーの役割について詳細に解析を行いました。
研究成果の概要
まず、活性化型Ras変異体を発現する変異細胞と正常上皮細胞を1:50の比率で混合培養し、細胞競合を惹起させたところ、混合培養した変異細胞内のオートファゴソームの数が単独培養時に比べて増加することが分かりました。さらに、オートファゴソームの分解を阻害してもオートファゴソーム数に変化はなかったことから、正常細胞に囲まれたRas変異細胞ではautophagic flux(*5)が停滞することが示唆されました。そこで、リソソームの機能を検討したところ、細胞競合下でのRas変異細胞ではリソソームの機能が著しく低下することを見出しました。
また、リソソームの機能を人為的に回復させると、オートファゴソームの蓄積が緩和され、さらには変異細胞の管腔側への排除率が有意に低下しました。オートファゴソームの形成を阻害しても同様に細胞競合の効率が低下したことから、オートファゴソームは形成される必要はあるが必ずしも分解されない、すなわちオートファゴソームの非分解機能が細胞競合を正に制御することを明らかにしました。
続いて、リソソームの機能低下ならびにオートファゴソームが蓄積する要因を調べるため、変異細胞に隣接する正常細胞による物理的排除圧の影響を検討しました。正常細胞内のフィラミン(*6)が変異細胞との境界面に集積し、これが変異細胞を管腔側へと押し上げる駆動力となることがこれまでに分かっていました(Kajita et al., Nat. Commun., 2014)。
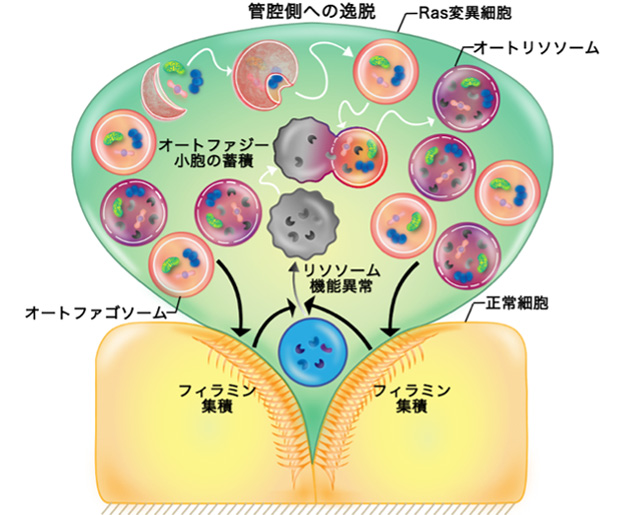
図1. 細胞競合におけるオートファジーの役割
正常細胞のフィラミン集積が変異細胞内のリソソーム機能低下ならびにオートファジー小胞の蓄積を誘引し、さらに蓄積したオートファジー小胞が正常細胞のフィラミン集積を促す。
そこで、正常細胞のフィラミンの機能を阻害したところ、変異細胞内のリソソームの機能低下とオートファゴソームの蓄積が観察されなかったことから、正常細胞からの物理的刺激が変異細胞内のオートファゴソームの分解異常の要因であることが分かりました。
さらに、オートファゴソームの形成が不全なRas変異細胞と正常細胞とを混合培養すると、正常細胞のフィラミン集積が阻害されたことから、変異細胞内に蓄積されたオートファゴソームが隣接する正常細胞のフィラミン集積を誘導し、さらにこのフィラミン集積が変異細胞のオートファゴソームの分解異常を促進するといった、ポジティブフィードバック機構が細胞競合を制御することを見出しました(図1)。
最後に、生体内の細胞競合におけるオートファジーの役割を評価するため、マウス上皮細胞層に活性化Ras変異細胞を少数産生することが可能な細胞競合マウスモデル(Kon et al., Nat. Cell Biol., 2017)を用いました。このマウスのRas変異細胞のみでオートファゴソームの形成を阻害させたところ、Ras変異誘導3日後の膵管において、Ras変異細胞の管腔への排除率が有意に低下しました。さらに、Ras変異誘導から[14]日経過すると、膵臓の水腫や胃や脾臓との癒着が認められました。また、膵管内には変異細胞が堆積し、膵管構造が破綻しており、周辺では炎症性細胞が蓄積していました。この結果より、オートファジーが不全になると細胞競合の効率が低下し、変異細胞が蓄積した結果、慢性膵炎様病変を引き起こすことが明らかとなりました(図2)。
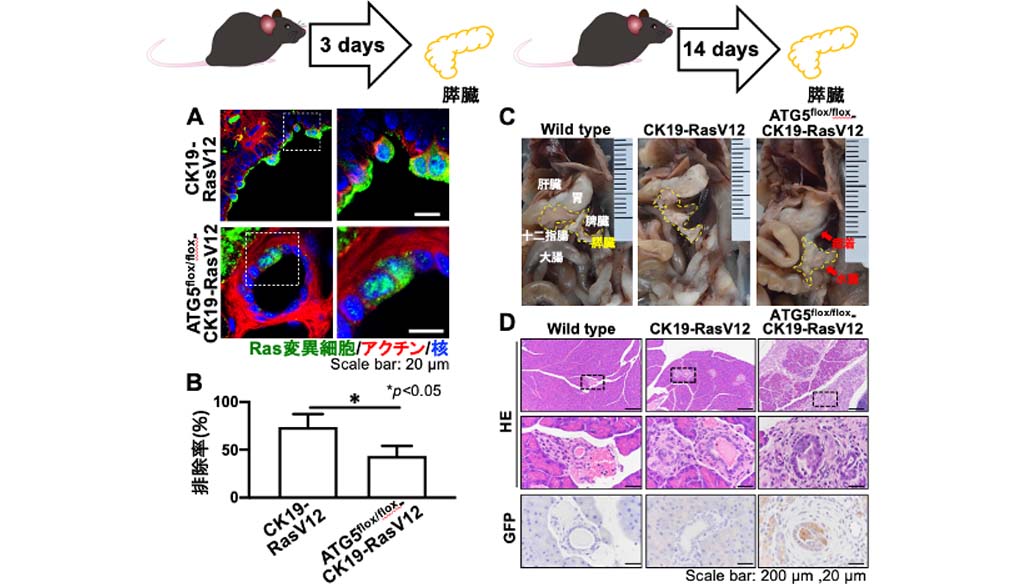
図2. Ras変異誘導3日後、14日後のマウス膵管での変異細胞の挙動
(A) Ras変異誘導3日後のRas単独変異マウス(CK19-RasV12)とオートファゴソーム形成不全Ras変異マウス(ATG5flox/flox-CK19-RasV12)の膵管の様子。ATG5flox/flox-CK19-RasV12マウスでは変異細胞の管腔への排除率が低下する(B)。(C) Ras変異誘導14日後の解剖写真。ATG5flox/flox-CK19-RasV12マウスでは膵臓の水腫や胃、脾臓との癒着が認められる。(D) Ras変異誘導14日後の膵臓のHE写真(上、中図)ならびにGFP(Ras変異細胞)の免疫染色画像(下図)。ATG5flox/flox-CK19-RasV12マウスでは変異細胞が膵管に堆積し、膵管構造が破綻する。また、外分泌組織の退行と炎症性細胞の蓄積が認められる。
今後の展望
本研究結果より、がん変異細胞が誕生したがん超初期段階において、オートファジーは細胞競合を介して変異細胞を排除し、生体内の恒常性維持に寄与することを明らかにしました。現在、オートファジーを標的とした抗がん剤開発が世界中で精力的に行われていますが、本成果よりがんの進行段階によってオートファジーの役割が異なることが分かったため、がんの進行時期を考慮した制がん戦略が今後必要になると思われます。
用語
*1 細胞競合
異なる性状の同種細胞が共在したとき、相対的に適応度の高い細胞が勝者細胞として生存し、他方が敗者細胞として排除される現象。
*2 リソソーム
真核生物が有する細胞内小器官で、様々な分解酵素を含む細胞内消化器官。
*3 オートファゴソーム
細胞質成分や細胞内小器官を包み込んだ二重膜構造体。リソソームと融合し、内容物が分解される。
*4 Ras
細胞の増殖、生存、分化、運動、接着を担う低分子量Gタンパク質。ヒトのがんで高頻度に活性化型変異が生じ、がん化を促進する。
*5 Autophagic flux
オートファゴソームが形成され、リソソームにて分解されまでの一連の過程。
*6 フィラミン
アクチン結合タンパク質で、アクチン繊維を架橋する。
論文情報
雑誌名
Cell Reports
論文タイトル
Non-degradable autophagic vacuoles are indispensable for cell competition
著者
Eilma Akter, Yukihiro Tasaki, Yusuke Mori, Kazuki Nakai, Kazuki Hachiya, Hancheng Lin, Masamitsu Konno, Tomoko Kamasaki, Kenji Tanabe, Yumi Umeda, Shotaro Yamano, Yasuyuki Fujita and Shunsuke Kon
DOI
研究室
昆研究室のページ:https://konshunsukelab.wixsite.com/rs-tus
昆講師のページ:https://www.tus.ac.jp/ridai/doc/ji/RIJIA01Detail.php?act=pos&kin=ken&diu=7036
東京理科大学について
東京理科大学:https://www.tus.ac.jp/
詳しくはこちら
